تغییرات متابولیک تغذیه ای موثر
بر تولید مثل گاوهای شیری پس از زایش
در طی دهه های اخیر دامداری های صنعتی با مقیاس بزرگ در حال افزایش هستند. افزایش تولید شیر (رکورد) عمدتا با انتخاب ژنتیکی بسیار زیاد و بهبود روند تغذیه حاصل شده است.
هرچند، در عملکرد تولید مثلی(RP) گاوهای پرتولید یک روند نزولی ثابتی مشاهده می شود. این کاهش در عملکرد تولید مثلی ممکن است به دلیل افزایش زمان تا اولین تلقیح، کاهش بروز رفتار فحلی، افزایش روزهای باز( تعداد روزها از زمان زایش تا ایجاد آبستنی مجدد) ، کاهش میزان گیرایی تلقیح مصنوعی (AIs)، و افزایش نرخ حذف ناشی از تولید مثل ضعیف باشد.
در کاهش RP عوامل متعددی از جمله عوامل ژنتیکی، استرس گرمایی و علل مرتبط با بیماری ها نقش دارند.
یک همبستگی منفی بین تولید شیر و تولید مثل وجود دارد، زیرا تولید بالای شیر در برخی مواقع حتی در صورت به خطر افتادن یا کاهش سلامت تولید مثل دام، حفظ می شود.
مصرف زیاد مواد مغذی توسط سیستم پستانی باعث تغییر در فیزیولوژی تولید مثل می شود. یک گاو شیرده با تولید بالا مقدار زیادی گلوکز مصرف میکند و در اوایل دوره پس از زایش در حالت بالانس منفی انرژی (NEBAL) قرار می گیرند.
با انتخاب برای تولید شیر بالا در پدران مورد استفاده برای اصلاح نژاد، امروزه شاهد کمرنگ شدن پایه ژنتیکی نژادهای اصیل در سراسر جهان هستیم و در نتیجه همراه باافزایش گاوداری های شیری،مشکلات مراقبت پس از زایش نیزافزایش پیدا کرده است.
در طول دوره پس از زایش، بالانس منفی انرژی شدید با بیماری های متابولیک بالینی یا تحت بالینی ظاهر می شود.
از این رو، ااین عامل بیماری، شایع ترین علت کاهش عملکرد تولیدمثلی در گاوهای شیری است. علاوه بر بیماری های عفونی، تب شیر، کتوز و سایر تغییرات تغذیه ای در کاهش عملکرد تولید مثلی نقش دارند.
تغییرات متابولیک تغذیه ای در طول دوره پس از زایش بر رشد و غالبیت فولیکول ها بر روی تخمدان ها و تخمک ریزی بعدی تأثیر میگذارند، در حالی که بیماریهای دستگاه تناسلی میتوانند مستقیماً بر لقاح، رشد جنین، جایگزینی و رشد جفت موثر باشند.
بازدهی تولیدمثل یک چالش اصلی در دوره های بهبودی (ریکاوری) طولانی تر تولید مثلی دام پس از زایش، فحلی خاموش (نشان ندادن علائم فحلی در حیوان)، نرخهای پایین آبستنی و همچنین عدم آبستنی در اوایل دوره شیردهی (در 60 روز اول پس از زایش) می باشد.
این شرایط و تغییرات به طور مکانیکی بر سه سیستم اصلی تنظیمکننده بدن دام تأثیر می گذارند:سیستم عصبی، سیستم غدد درون ریز و سیستم گردش خون به همراه سیستم ایمنی.
حدود دو سوم از ناهنجاری های تولید مثلی در ماه اول پس از زایش مشاهده می شود.
در مجموع، این عوامل به طور مستقیم یا غیرمستقیم بر رشد فولیکولها، جنین و جفت تأثیر میگذارند .
هدف این مقاله درک صحیح این رویدادها، روابط متقابل آنها و پیامدهای کاهش و عملکرد ضعیف تولیدمثل است.
تمرکز اصلی این مقاله بر اختلالات متابولیک تغذیه ای و ارتباط پیچیده آنها با پیامدهای تولیدمثل در گاوهای شیری خواهد بود.
ویژگی های تغذیه ای، بیماری های متابولیک و تولید مثل گاوهای شیری
نشخوارکنندگان مانند گاوها برای تامین انرژی مورد نیاز خود غذا را تخمیر می کنند و گلوکونئوژنز در کبد برای سنتز لاکتوز در غدد پستانی نقش اساسی دارد.
در طول دوره پس از زایش، نوساناتی در ماده خشک مصرفی (DMI) وجود دارد. کاهش قابل توجهی در DMI در 10 روز آخر زایش مشاهده میشود و به دنبال آن افزایش معنی داری پس از آن وجود دارد، که برای رفع نیاز افزایش یافته مواد مغذی و انرژی گاوهای شیری پس از زایش کافی نیست.
اوج شیردهی پس از زایش معمولاً پس از 4 تا 6 هفته مشاهده می شود، در حالی که پیک DMI در هفته 8 تا 10 می باشد. از این رو، گاوها حداقل 50 روز پس از زایش در حالت بالانس منفی انرژی (NEBAL)هستند.
طبق برخی مطالعاتDMI پایین پیش از زایش و توازن انرژی با هضم پس از زایش و اختلالات متابولیکی مرتبط است.
مصرف خوراک کافی و تأمین انرژی مورد نیاز در طول دوره قبل و بعد از زایش perinatal)) از اهمیت بالایی در جهت سلامتی و عملکرد تولید مثلی برخوردار است.
علاوه بر DMI، نمره وضعیت بدن (BCS) به طور گسترده ای برای ارزیابی بالانس انرژی، سلامت و نتایج تولید مثل در گاوهای شیری در شرایط پس از زایش استفاده می شود.
BCS بالاپیش از زایش با افزایش خطر مشکلات متابولیکی پس از زایش همراه است، در حالی که مطالعات دیگر نشان می دهد که BCS پایین پیش از زایش مسئول اختلالات متابولیکی و تولید مثل پس از زایش است.
دلیل این تضاد در مطالعات اساساً به دلیل تغییرات متابولیسم انرژی پس از زایش در ارتباط با موبیلیزاسیون (بسیج) بافت چربی می باشد که در آن BCS بالاتر پیش از زایش (چاقی) با ناهنجاری های متابولیکی پس از زایش و بازده پایین تولید مثل مرتبط است .
علاوه بر این، کاهش BCS قبل از زایش به میزان 0/5 نمره یا بیشتر میتواند بر سطوح کلسیم خون در دوره قبل یا بعد از زایش تأثیر منفی بگذارد و گاوها را مستعد خطر کتوز و تأخیر در آبستنی کند.
علاوه بر این، BCS بالا پیش از زایش با وزن پایین بدن گوساله مرتبط بود. می توان نتیجه گرفت که BCS پایین قبل از زایش و افزایش بیش ازحد نمره بدنی (BCS بالاتر) هر دو برای بازده تولید مثل پس از زایش نامطلوب هستند.
گاوها با افزایش بیش ازحد نمره بدنی دارای سطوح mRNA پایین تر TNFα و سطوح mRNA بالاتری از گاما-گيرنده هاي فعال کننده تکثير پراکسي زوم ها (PPAR) در بافت های چربی در طول پس از زایش بودند، در حالی که مسیر پروتئین کیناز فسفریله (AKT) B مربوط به تغییرات متابولیکی شدید از طریق سیگنال دهی ضعیف انسولین در بافت چربی نیز تنظیم می شود.
تنظیم همزمان پدیده مسیر سیگنال سیتوکین التهابی زیادو مسیر سیگنال AKT به طور هم افزایی متابولیسم انرژی را افزایش می دهند.
می توان پیشنهاد کرد که کنترل توازن انرژی از طریق متابولیت های سرم می تواند به فیزیولوژی تغذیه پس از زایش و پیامدهای نهایی آن در عملکرد تولید مثل کمک کند.
بالانس منفی انرژی پس از زایش با غلظت پایین گلوکز و انسولین خون و غلظت اجسام کتونی و غلظت اسیدهای چرب غیر استریفیه (NEFA) بالا مشخص می شود.
با این حال، بالانس منفی انرژی همراه با بیماریهای متابولیک تغذیهای مانند کتوز، بازگشت رحم به حالت اولیه و فرایند طبیعی تولید مثل را به تاخیر میاندازد و منجر به طولانیتر شدن مدت زمان اولین تلقیح پس از زایش و افزایش فاصله گوساله زایی شود.
بررسی ها تایید میکند که بیماریهای متابولیک تغذیهای پس از زایش، علل اصلی اختلالات تولید مثل پس از زایش در گاوهای شیری هستند.
بیماریهای متابولیکی تغذیهای، بیماری های پیچیده تولیدی «production diseases » هستندکه میزان بروز آنها در گاوهای شیری صنعتی بالا می باشد که علاوه بر زیان های اقتصادی مستقیم ناشی از کاهش تولید شیر، می توانند تأثیر منفی درازمدتی بر فیزیولوژی گاوها، به ویژه عملکرد تولید مثلی آنها داشته باشند.
در یک مطالعه روی 7500 گاو هلشتاین در نزدیکی دوره قبل از زایش نشان داد که در عرض 21 روز پس از زایش، حدود یک سوم گاوها حداقل یک بیماری متابولیک تحت بالینی یا بالینی داشتند.
علاوه بر این، میزان لقاح 45 روزه 7 درصد و وتولید شیر 14 درصد کاهش یافت و همچنین نرخ حذف از 22/6 درصد (بدون بیماری بالینی) به 35/7 درصد (یک بیماری بالینی) و 53/8 درصد (بیش از سه مورد بالینی) برای گاوهای دچار بیماری متابولیک افزایش یافت.
در مطالعه دیگر، میزان وقوع کتوز تا 26 درصد در شصت روز اول زایش نشان داده شد. مطالعهای که در 12 کشور از چهار قاره انجام شد نشان داد که میانگین شیوع کتوز تحت بالینی در 21 روز اول پس از زایش 24/1٪ بودکه از 8/3٪ تا 40/1٪ متغیربود.
نخستین شیردهی پس از زایش به قیمت کاهش عملکرد تولیدمثلی حفظ می شود. سازوکار مرتبط به بالانس منفی انرژی را می توان با سطوح پایین انسولین توضیح داد که باعث افزایش هورمون های رشد (GHs) می شود و به نوبه خود NEFA موبیلیزاسیون (بسیج) را باعث می شود.
با این حال، در همان زمان، کاهش فراوانی گیرنده های GH کبدی وجود دارد که از بازخورد منفی از طریق IGF-1 جلوگیری می کند، در حالی که حضور NEFA ها به طور مداوم درنتیجه انسولین پایین از طریق کاتکولاآمین ها افزایش می یابد.
از آنجایی که لیپولیز به تقاضای شیردهی کمک می کند علت اصلی کاهش BCS در گاوهای پس از زایش است. بنابراین، BCS پس از زایش یک اندازه گیری غیرمستقیم متابولیسم چربی است و با تعادل انرژی گاوها ارتباط دارد.
این تغییرات متابولیک که در بالا ذکر شدند با واسطه تغییرات پیچیده غدد درون ریز پیامدهای بیشتری برای تخمک ریزی، تخمک ها و جسم زرد دارند. ارتباط بیشتر این تغییرات با عملکرد تولید مثلی مربوط به غلظت کم انسولین و فاکتور رشد شبه انسولین 1 (IGF-1) است که باعث تغییرات بیوشیمیایی فولیکولی در تخمدان ها می شود که در نتیجه بر ترشح هورمون لوتئینه کننده (LH) و استرادیول (E2) تأثیر می گذارد.
این کاهش در ترشحات LH و E2 به نوبه خود در نهایت منجر به تاخیر در شروع مجدد چرخه فحلی می شود. از سوی دیگر، نشان داده شده است که بالانس منفی انرژی با غلظت پایین پروژسترون نیز مرتبط است، که تأثیر منفی بر نتیجه اولیه آبستنی دارد.
در ادامه بحث، نشان داده شده است که غلظت بالای NEFA خون به طور منفی با توانایی رشد تخمک های بارور شده مرتبط است. به طور کلی، افزایش بیش از 0/55 میلی مول در لیتر سطح NEFA پلاسما به عنوان علامت جدی بالانس منفی انرژی پس از زایش در نظر گرفته می شود.
از آنجایی که NEBAL به خودی خود دارای پیامدهایی برای ریکاوری زودهنگام تولید مثل است همچنین می تواند به عنوان یک علت اصلی بیماری های مختلف پس از زایش در نظر گرفته شود.
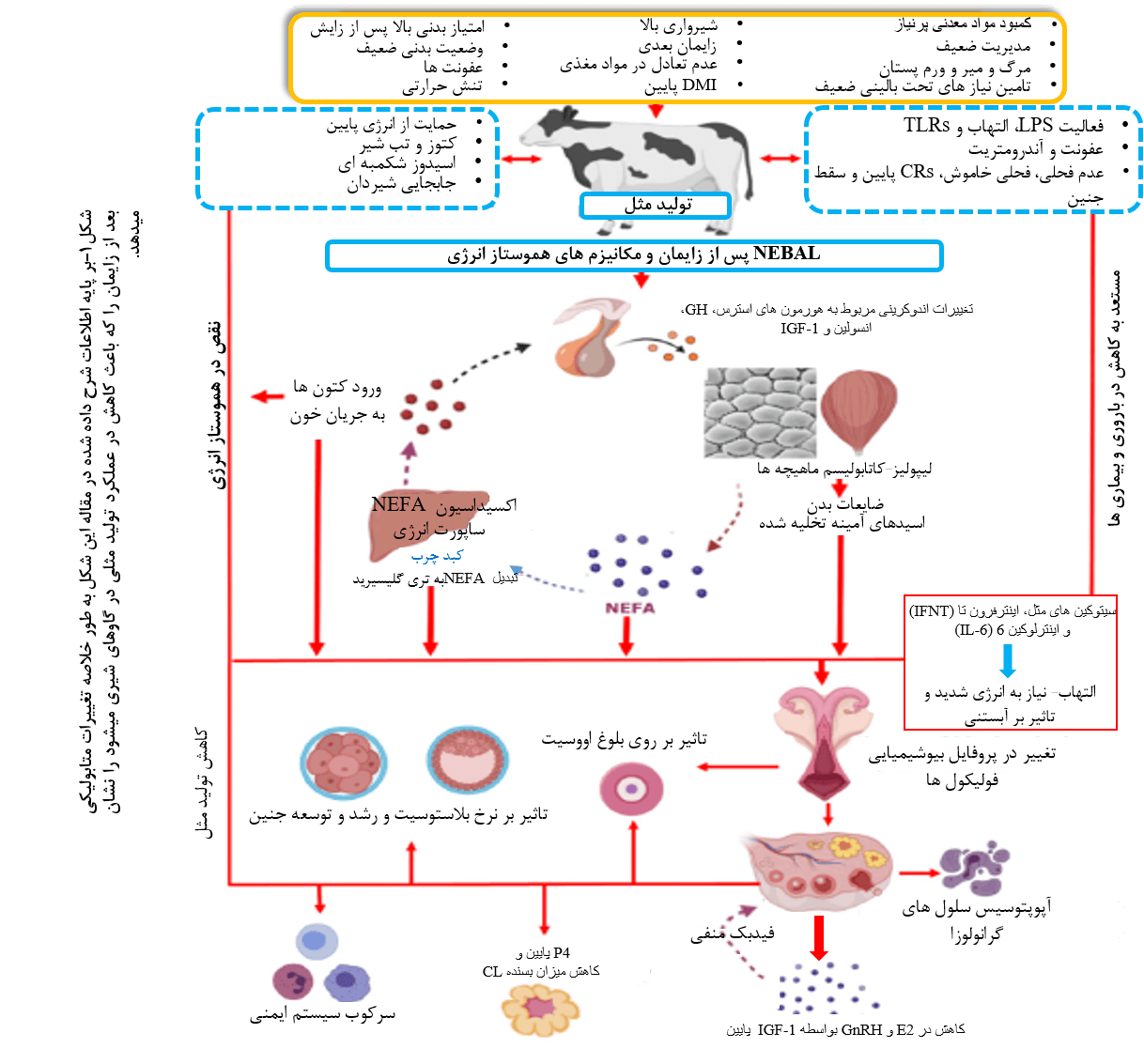
بر اساس بحثهای این مقاله مروری، شکل 1 مکانیسمهای متابولیکی و غدد درون ریز مختلف که در کاهش عملکرد تولیدمثلی پس از زایش در گاوهای شیری نقش دارند، را خلاصه میکند.
راهکارهایی برای به حداقل رساندن بروز شدید بالانس منفی انرژی پس از زایش توصیه شده است. مدیریت گاو خشک باید بر روی تغذیه با جیره های غنی از انرژی در طول 3 تا 4 هفته قبل از زایش متمرکز شود تا رشد جنین، کاهش DMI و مشکلات هنگام زایش را تحت الشعاع قرار دهد.
این پدیده افزایش محتوای انرژی رژیم را می توان با کاهش مصرف DMI و زمان نشخوار در طی 3 هفته آخر آبستنی تفسیرکرد. یک جیره غذایی کنترل شده از نظر انرژی قبل از زایش در حد نیازهای تخمین زده شده ، به طور اساسی از خطر بالانس منفی انرژی پس از زایش جلوگیری می کند. ی
ک جیره غذایی بسیار غلیظ از نظر انرژی قبل از زایش باعث افزایش تجمع چربی، کاهش DMI و همچنین افزایش خطر مشکلات سلامتی در گاوهای شیری پس از زایش می شود.
به طور مشابه، دیگر محققان نشان داده اند که افزایش انرژی در جیره غذایی قبل از زایش می تواند منجر به افزایش بسیج یا موبیلیزاسیون NEFA و تجمع تری گلیسیرید (TG) در کبد گاوهای پس از زایش شود، و این در حالی است که جیره غذایی با انرژی کنترل شده قبل از زایش باعث بهبود عملکرد ایمنی گاوهای شیری پس از زایش می شود.
بنابراین، مدیریت دقیق تغذیه از طریق نظارت بر محتوای انرژی خوراک و ارزیابی BCS گاوهای قبل از زایش، یک کلید اساسی برای موفقیت انتقال دوره های قبل و پس از زایش است.
او شیری بعد از زایش تنش های بسیار زیادی را متحمل می شود که شامل تنش زایمان ناشی از نیروی کارگری، افزایش تقاضای نیازهای شیردهی، تنش های گرمایی، کاهش مصرف مادهی خشک (DMI)، تغییرات رحم و شروع چرخه تولید مثلی می باشد.
به این دلیل گاوهای شیری معمولاً بعد از زایمان در شرایط بالانس منفی انرژی قرار می گیرند. بالانس منفی انرژی به تغییرات متابولیکی و اندوکرینی منجر می شود که آغازگر آن انسولین پایین، تقاضای بالای گلوکز، کاهش فاکتور رشد انسولین (IGF-1) و میزان بالای فعالیت هورمون رشد (GH) است، که منجر به پاسخ افزایش غلظت اسیدهای چرب غیر استریفیه (NEFA) می شود.
اسیدهای چرب غیر استریفیه برای حمایت از انرژی در کبد اکسیده می شوند و منجر به بروز کتوز شده و در نهایت به علت تجمع تریگلیسیریدها (TGs) به کبد چرب می انجامد.
وضعیت بدنی نامطلوب قبل از زایش به عنوان عامل مستعدکننده بسیج شدید منابع چربی بدن به فرم اسیدهای چرب غیر استریفیه عنوان شده است.
بسیج چربی و متابولیسم پروتئین منجر به تخلیه بیشتر اسیدهای چرب و آمینواسیدهای مورد نیاز برای تولیدمثل و سلامت بدن می شود. این تغییرات علت اولیه بیماری های متابولیکی ثانویه از جمله هیپوکلسیمی، اسیدوز شکمبه و جابجایی شیردان است.
علاوه بر این، در نهایت منجر به تغییراتی در پروفایل بیوشیمیایی فولیکول های تخمدان، اووسیت های بارور شده، توسعه جنین، جسم زرد (CL) و رحم شده که در نهایت منجر به نرخ پایین آبستنی (CRs) شده، در حالی که در کنار این تغییرات ، تغییرات اندوکرینی در محور هیپوفیز- هیپوتالاموس- تخمدان شامل تغییرات در استروژن (E2)، گنادوتروپین ها (GnRH)، هورمون لوتئینی کننده (LH) و پروژسترون (P4) نیز دیده می شود.
بعلاوه بر این، این تغییرات ذکر شده سیستم ایمنی گاوهای شیری را بعد از زایش از طریق فعال سازی لیپوپلی ساکاریدها (LPS)، سیتوکین ها و گیرنده های Toll-like(TLRs) تحت تاثیر قرار می دهد. این پدیده گاوها را مستعد عفونت و التهاب کرده و بنابراین در کاهش نرخ آبستنی نقش دارند.
ترجمه : مهندس فرشته قدیمی ، منبع